Decadimenti circostanti

Dopo il primo articolo ho pensato: tutto decade? La fisica e le persone tendono a dare un significato diverso a questa parola, ma una cosa in comune c’è.
1 Tutto è radioattivo?
Per noi una cosa decade se viene abbandonata, se perde vitalità, diventa vecchia, passata. Ci sono cose che possiamo recuperare, a cui possiamo dare una nuova vita con una “sistemata”, e altre che invece sono perse per sempre. In fisica ci sono isotopi stabili, che nessuno ha mai visto decadere, sempre perfetti, e isotopi instabili, che invece decadono, prima o poi muoiono… che perdiamo.
Prima di avviarci al cuore dell’articolo, penso sia giusto fornirvi tutti gli strumenti necessari alla sua comprensione. Creerò quindi via via delle schede tecniche apposite con gli approfondimenti teorici che servono. Iniziamo subito con uno sugli isotopi. Cosa sono?
1.1 Isotopi
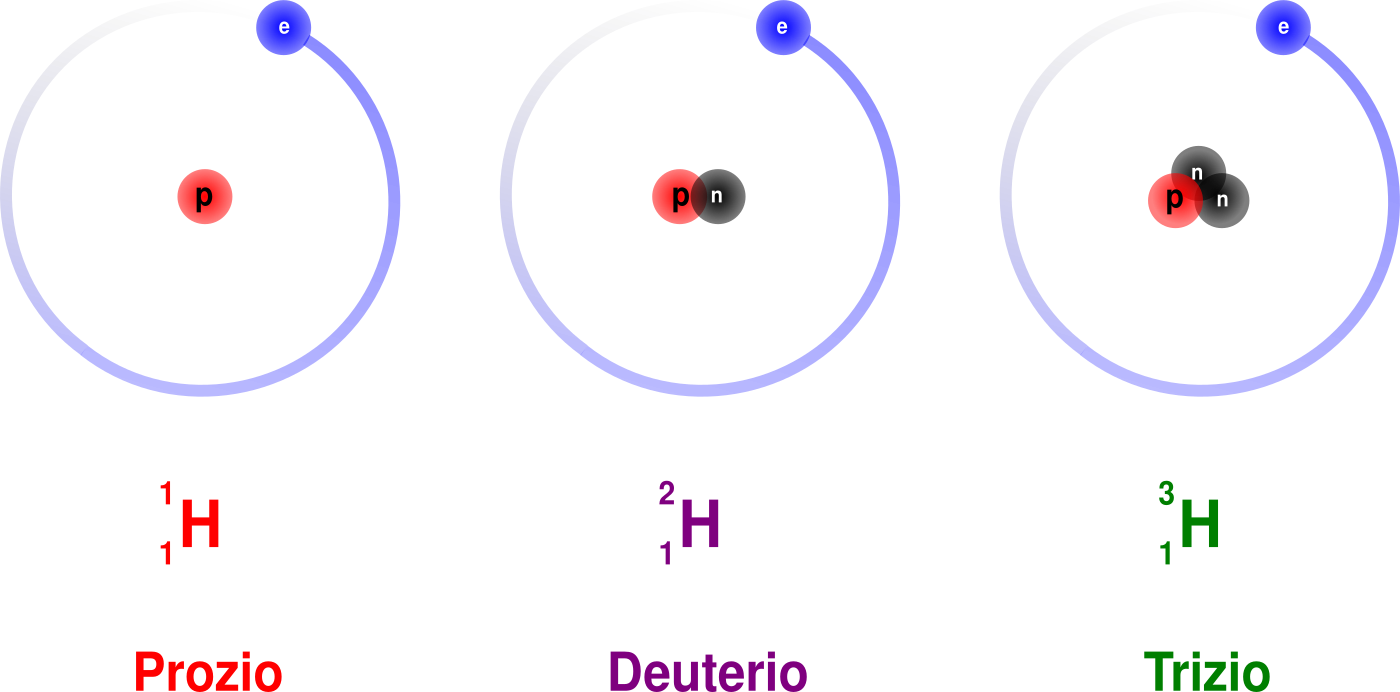
Ogni elemento può avere diversi isotopi, cioè diverse “versioni di sé”, che si contraddistinguono per un diverso numero di neutroni all’interno del nucleo atomico. Ciò che fa l’elemento quindi è il numero di protoni. Ad un certo numero di protoni corrisponde un unico e solo elemento, i neutroni invece possono variare, creando i diversi isotopi. Facciamo un esempio. Consideriamo il primo elemento della tavola periodica: l’idrogeno. In natura sono presenti tre isotopi dell’idrogeno: prozio, deuterio, trizio.
$\space$
$\space$
Come vediamo dalla figura, l’isotopo Prozio ha nel nucleo un solo protone, l’isotopo Deuterio ha un protone e un neutrone, l’isotopo Trizio due neutroni ed un protone. Tutti e tre sono atomi di idrogeno, in quanto hanno un solo protone, ma si distinguono per il numero di neutroni.
Nota: nella formula $ _{1}^{3}H$ l’apice, “3” nel caso del trizio, si chiama numero di massa e rappresenta la somma di neutroni e protoni nel nucleo. Il pedice invece si chiama numero atomico e rappresenta il numero di protoni dell’elemento.
2 Si
Tutti gli elementi hanno isotopi, e quasi tutti hanno almeno un isotopo instabile, cioè che decade, radioattivo. Puoi vedere qui la lista di tutti gli isotopi conosciuti dei vari elementi.
Di solito gli isotopi instabili di un elemento sono presenti in natura con percentuali molto basse rispetto agli isotopi stabili, ma ci sono! Questo ci consente di dire che tutto quello che ci circonda è in realtà radioattivo. Ci sono degli atomi, intorno a noi e dentro di noi, che stanno decadendo proprio in questo momento. Facciamo un esempio.
2.1 Il potassio è radioattivo
Mentre scrivo la temperatura esterna si aggira attorno ai 32 gradi, fa molto caldo e ci viene consigliato spesso di assumere integratori di sali minerali. Tra questi abbiamo sicuramente tutti sentito nominare almeno una volta il potassio. Analizziamo allora il potassio, i suoi isotopi, e studiamone il decadimento. Riportiamo tutti i dati in una tabella.
| Isotopi | Abbondanza in natura | $t_{\frac{1}{2}}$ (anni) |
|---|---|---|
| $ _{19}^{39}K$ | 93,26 % | stabile |
| $ _{19}^{40}K$ | 0,01 % | $1,277 \cdot 10^{9}$ |
| $ _{19}^{41}K$ | 6,73 % | stabile |
Come vediamo, l’isotopo instabile del potassio è il $ _{19}^{40}K$, presente in natura con una percentuale dello $0,01 %$ avente tempo di dimezzamento di $1,277 \cdot 10^9$ anni.
Quanto potassio $ _{19}^{40}K$ c’è nel nostro corpo? Nel corpo umano mediamente ci sono 160 grammi di potassio. Dunque lo 0,01% è $ _{19}^{40}K$: 0,016 grammi. Una piccola parte del potassio presente nel nostro corpo è radioattiva. Dobbiamo preoccuparcene? Vediamo quanti decadimenti di potassio si verificano ogni secondo nel nostro corpo.
2.2 Legge del decadimento
Come vediamo dalla tabella, il tempo di dimezzamento di $ _{19}^{40}K$ è di $1,277 \cdot 10^9$ anni. Ma cosa significa esattamente questa cosa? Trascorso questo preciso periodo di tempo vedremo la metà del campione di potassio decadere? No, il decadimento è un processo spontaneo e naturale, può avvenire in qualsiasi momento. Il tempo di dimezzamento è una statistica, una media, studiata sui singoli isotopi, che ci dice dopo quanto tempo approssimativamente un campione di materiale si sarà dimezzato. Dopo quanto tempo si può verificare quindi un singolo decadimento? Per saperlo sfruttiamo la legge del decadimento:
$$ N(t) = N_{0}e^{-\lambda t} $$
nella quale $N(t)$ indica gli isotopi non ancora decaduti, $N_{0}$ gli isotopi iniziali, $\lambda$ la costante di decadimento, diversa da isotopo a isotopo. Siccome vogliamo sapere quanti sono gli isotopi **decaduti** nel tempo, andiamo a fare la differenza tra gli isotopi iniziali e quelli non ancora decaduti:
$$ D(t)=N_{0}-N(t)=N_{0}(1-e^{-\lambda t}) $$
Sapendo che
$$ \lambda = \frac{Ln(2)}{t_{1/2}} $$
e che in 0.016g di $ _{19}^{40}K$ ci sono all’incirca $2,47 \cdot 10^{20}$ isotopi, possiamo calcolare quanti ne decadono.
Nel nostro corpo, ogni secondo, ci sono all’incirca 4250 decadimenti dei soli isotopi di potassio!
2.3 Banana Equivalent Dose
Oltre che nel nostro corpo, la stessa cosa accade negli alimenti. Le banane ad esempio sono ricche di potassio, e per lo stesso motivo risultano radioattive! Addirittura è stata creata una unità di misurata basata sulla quantità di radiazione emessa da una banana, equivalente a circa $0.1 \mu Sv$, chiamata appunto BED (Banana Equivalent Dose), che da sola costituisce l'1% delle radiazioni a cui siamo esposti quotidianamente.
Non c’è però bisogno di preoccuparsi, nemmeno se mangiamo tante banane. Per assumere una dose letale di radiazioni da banane dovremmo mangiarne 35 milioni tutte insieme.
3 Decadimento circostante
Nei prossimi post andremo ad approfondire le altre fonti di radioattività ambientale a cui siamo esposti ogni giorno, con questo articolo volevo solo iniziare a far notare come tutto quello che ci circonda è radioattivo, e che radioattivo non vuol dire per forza pericoloso. Fa parte della natura trasformarsi, cambiare, essere in perenne mutamento.
La cosa bella è proprio questa. Quando guardiamo un amico*, un oggetto, un animale, magari pensiamo che questo* stia cambiando, stia crescendo, stia invecchiando, ma non pensiamo mai al fatto che tutto parta già dagli atomi che lo costituiscono, dai mattoncini fondamentali di cui tutto è fatto, che sono in perenne movimento e trasformazione.
Fateci caso la prossima volta :)